از ژنتیک چه میدانید؟
حتما تا به حال واژه های DNA، کروموزوم و کاریوتایپ را به خصوص در آزمایشات قبل از ازدواج یا تست های پیش از تولد نوزاد، شنیده اید. آیا با این مفاهیم آشنا هستید؟ برخی بیماری های ژنتیکی مربوط به تغییر در تعداد یا مشکلات ساختاری کروموزوم هاست، بنابراین آنالیز آنها از اهمیت ویژه ای در پیشگیری اختلالات کروموزومی برخوردار است. اگر مایل به درک بهتر این مفاهیم از لحاظ زیست شناسی و ژنتیکی هستید، این مقاله را از دست ندهید. در این مقاله سعی شده توضیحاتی به زبان ساده برای دی ان ای، کروموزوم، کروماتین و اهمیت آنها ارائه شود.
آنالیز کروموزوم ها
تجزیه و تحلیل کروموزوم، آزمایشی برای بررسی آن در نمونه ای از سلول ها است که به شناسایی ناهنجاری های ژنتیکی مرتبط با کروموزوم ها به عنوان علت یک بیماری کمک می کند. در آنالیز کروموزوم ها یا به اصطلاح تهیه کاریوتایپ، کروموزوم ها از لحاظ ساختار و تعداد مورد بررسی قرار می گیرند. معمولاً این آزمایش در آزمایشگاه طبی بر روی نمونه خون انجام می شود. در دوران بارداری، کروموزوم های جنین از طریق تست NIPT و در صورت لزوم به وسیله آمنیوسنتز مورد بررسی قرار می گیرند. NIPT دی ان ای جنینی که در گردش خون مادر وجود دارد را بررسی می کند و آمنیوسنتز یک روش تهاجمی جهت بررسی محتوای ژنتیکی جنین است. در این روش از مایع آمنیوتیک نمونه برداری می شود. همچنین این آزمایشات ممکن است توسط پزشک یا مشاور ژنتیک برای تعیین علل ژنتیکی ناتوانی ذهنی، تأخیر در رشد، اختلالات طیف اوتیسم، نقص مادرزادی یا کوتاهی قد تجویز شود. برای درک بهتر کروموزوم ها به توضیح مفاهیم پایه در این رابطه می پردازیم.
سلول و تقسیم سلولی
سلول ها کوچکترین واحد ساختاری موجودات زنده هستند. هر سلول کارایی و عملکرد خاص خود را دارد. سلول های سازنده بدن انسان دارای یک هسته و اندامک دیگر هستند که کارهای مختلفی را انجام می دهند. هسته سلول حاوی کل ماده ژنتیکی آن سلول و در نتیجه تعیین کننده هویت و عملکرد آن است. سلول ها به دلایل مختلفی تقسیم می شوند و دو سلول جدید ایجاد می کنند. برای مثال هنگامی که دست شما می برد، تعداد زیادی از سلول های پوست و بافت زیرین آن میمیرند، بنابراین در جهت ترمیم زخم، سلول ها در این ناحیه شروع به تقسیم می کنند. ایجاد سلول های جنسی را می توان به عنوان نوعی دیگر از تقسیم سلولی نام برد. هنگامی که یک سلول تقسیم می شود، هر سلول دختر باید حتما یکی نسخه کامل از مواد ژنتیکی سلول مادر را داشته باشد. اشتباهات هنگام کپی برداری یا تقسیم نابرابر ماده ژنتیکی بین سلول ها می تواند منجر به تولید سلول هایی ناسالم یا ناکارآمد شود. این اختلالات می توانند در سطح DNA یا در سطح کروموزوم باشند. اما دقیقاً این ماده ژنتیکی چیست و در طول تقسیم سلولی چگونه رفتار می کند؟
DNA و ژنوم ها
احتمالا تا به حال شنیده اید که زبان کامپیوتر ها صفر و یک است. یعنی تمام اطلاعات به صورت رمزهای حاوی صفر و یک در کامپیوتر ذخیره می شوند. در سلول های بدن ما نیز چیزی شبیه به این صفر و یک ها وجود دارد. DNA یا دئوکسی ریبونوکلئیک اسید ها بلوک های سازنده ماده ژنتیکی انسان هستند. 4 نوع دئوکسی ریبونوکلئیک اسید وجود دارد و از کنار هم قرار گرفتن آنها رشته DNA و رمز های ژنتیکی ایجاد می شوند. برای مثال رمز های ژنتیکی می توانند رمزگردانی شده، پروتئین ها را بسازند. در انسان، DNA تقریباً در تمام سلولهای بدن یافت می شود و دستورالعملهای لازم برای رشد، عملکرد و واکنش سلول به محیط اطرافش را فراهم می کند. اغلب می توان گفت که هر ژن حاوی اطلاعات مربوط به ساخت یک پروتئین یا سایر مولکول های حیاتی سلول است.
مجموعه کل DNA یک سلول را ژنوم آن می نامند. تمام سلولهای یک موجود زنده (به استثنای چند مورد) حاوی DNA یکسانی هستند. تمام سلول ها ژنوم یکسانی دارند اما تنها برخی از ژن ها در هر سلول، بسته به عملکرد و خصوصیات آن روشن و فعال بوده، برخی دیگر در زمان های خاصی فعال می شوند. بنابراین سلول ها در بافت های مختلف، خصوصیات و عملکردهای خاص خود را دارند.
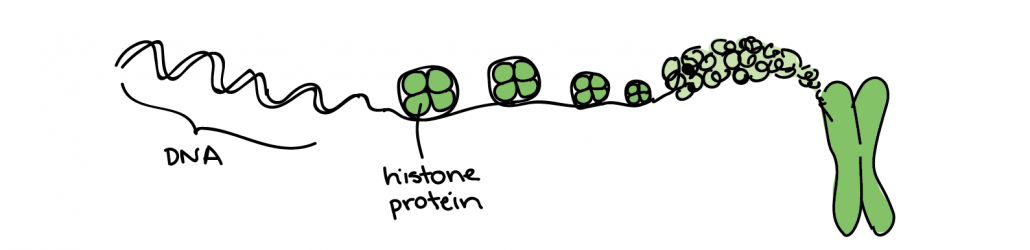
کروماتین و کروموزوم
در یک سلول، DNA معمولاً به صورت برهنه وجود ندارد. یعنی رشته دی ان ای با میانکش با پروتئین های خاص سازمان یافته می شود و ساختار خاص خود را می یابد. از آنجایی که اطلاعات زیادی در ژنوم سلول ذخیره می شود، بنابراین رشته های دی ان ای حاوی این اطلاعات بسیار طویل هستند. برای گنجاندن ماده ژنتیکی در هسته سلول پروتئین های خاصی به نام هیستون ها وجود دارند هیستون ها علاوه بر سازماندهی و فشرده سازی DNA، نقش مهمی در تنظیم بیان ژن ها دارند. مجموعه DNA به علاوه هیستون ها و سایر پروتئین های ساختاری را کروماتین می نامند. در بیشتر عمر سلول، اگر هسته آن را زیر میکروسکوپ مشاهده کنید کروماتین وجود دارد. در این حالت، DNA برای ماشین آلات سلولی (مانند پروتئین هایی که DNA را می خوانند و کپی می کنند) به راحتی قابل دسترسی است. کروماتین همچنین می تواند متراکم شود. فشرده شدن و به اصطلاح بسته بندی کروماتین زمانی اتفاق می افتد که سلول در شرف تقسیم است. این روند در چند سطح فشرده سازی انجام می شود و در نهایت کروموزوم ها که فشرده ترین حالت DNA هستند، در مراحل تقسیم سلولی قابل مشاهده می باشند.
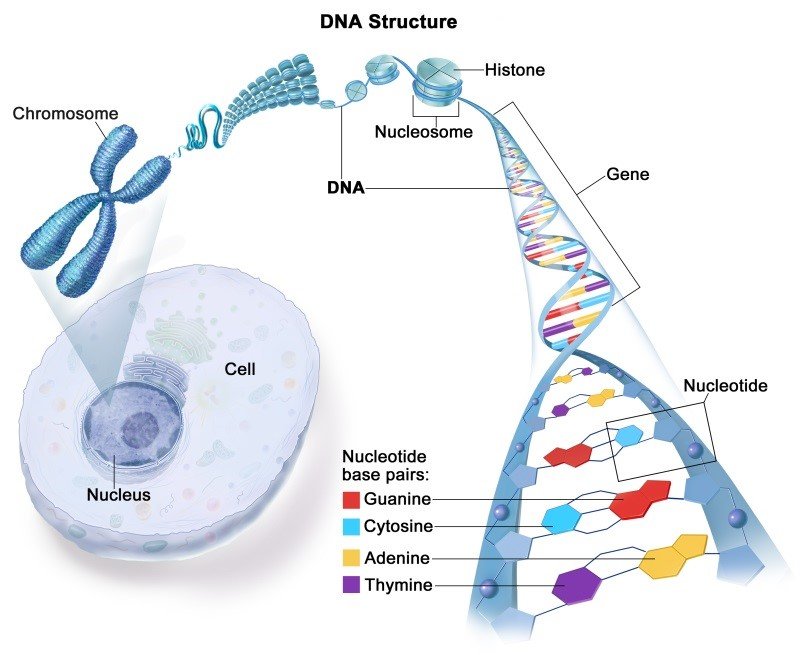
کروموزوم ها
هر گونه از موجودات تعداد مشخصی از کروموزوم ها را دارد. به عنوان مثال، انسان دارای 46 کروموزوم در یک سلول معمولی بدن دارد. این 46 عدد به صورت 23 جفت در سلول وجود دارند (به استثنای کروموزوم های جنسی که جنسیت را مشخص می کنند و به صورت XX (ماده) و XY (نر) می باشند). هنگام لقاح سلول جنسی نر و ماده که هر کدام 23 عدد کروموزوم دارند، هر فرد 23 عدد کروموزوم از مادر و 23 تا از پدر به ارث می برد و اینگونه سلول تخم 46 کروموزومی شکل می گیرد. بنابراین، برای هر جفت کروموزوم همولوگ (مشابه) در ژنوم شما، یکی از همولوگ ها از مادر شما و دیگری از پدر شما می آید.
دو کروموزوم موجود در یک جفت همولوگ بسیار شبیه به هم هستند و اندازه و شکل یکسانی دارند. از همه مهمتر، آنها اطلاعات ژنتیکی یکسانی را حمل می کنند؛ یعنی ژن های با عملکرد اصلی یکسان در مکان های مشابه دارند. با این حال، کروموزوم های همولوگ لزوما نسخه های مشابه ژن ها را ندارند. دلیل این امر این است که شما ممکن است دو نسخه ژن مختلف از مادر و پدرتان به ارث برده باشید.
به عنوان یک مثال واقعی ژنی را در کروموزوم شماره 9 در نظر میگیریم که گروه خونی A،B ، AB یا Oرا مشخص می کند. در سلول های همه افراد سالم، ژن مربوط به گروه خونی در قسمت خاصی از کروموزوم 9 قرار دارد. اما گروه های خونی متفاوت است. مثلا فردی که گروه خونی AB دارد، بر روی یکی از کروموزوم های شماره 9 او اطلاعات مربوط به A و بر روی جفت آن اطلاعات مربوط به B قرار دارد.
اختلالات کروموزومی:
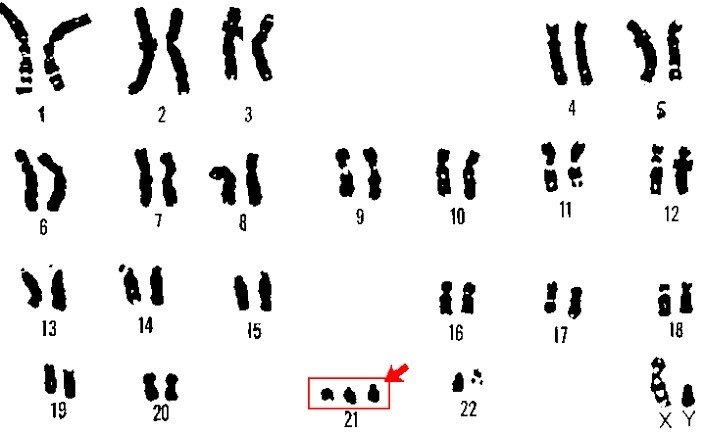
اختلالات کروموزومی انواع متعددی دارند برای مثال ممکن است در تعداد طبیعی آن ها تغییر ایجاد شود یا بخش هایی از یک کروموزوم حذف یا به آن اضافه شود. اختلالات عددی یکی از مهم ترین انواع آن هستند که در غربالگری های پیش از تولد اهمیت ویژه ای دارند. سندرم داون یکی از این بیماری ها به شمار می آید که در آن فرد سه کروموزوم 21 دارد. به عبارتی دیگر، هر فرد سالم یک جفت کروموزوم 21 دارد اما در افراد مبتلا به سندرم داون این عدد به 3 رسیده است و بیماران یک کروموزوم اضافی دارند. برای مطالعه بیشتر در این زمینه به مقاله مربوط به کاریوتایپ در همین سایت مراجعه فرمایید.
منابع:





















ما را دنبال کنید!